Auteur:
Louise Ward
Denlaod Vun Der Kreatioun:
11 Februar 2021
Update Datum:
1 Juli 2024

Inhalt
D'Gréisst vun engem Atom ass sou kleng datt et schwéier ass d'Atomzuel vun enger chemescher Verbindung ze moossen. Fir eng Quantitéit u Substanze genau ze moossen, benotze Wëssenschaftler eng Molmol fir eng spezifizéiert Zuel vun Atomer duerzestellen. Eng Mol Substanz ass definéiert als gläichwäerteg mat der Zuel vu Kuelestoffatomer, déi an 12 Gramm vum 12 Kuelestoffisotop enthale sinn, wat ongeféier 6.022 x 10 Atomer ass. Dëse Wäert gëtt d'Avogadro Nummer genannt, oder d'Avogadro Konstant. Dëst gëtt och als Zuel vun Atomer an 1 Mol vun all Element bezeechent, an 1 Mol vun der Mass vun enger Substanz gëtt als Molmass vun där Substanz bezeechent.
Schrëtt
Method 1 vun 2: Berechent déi molmass vun engem Element
Definitioun vu Molmass. Molmass vun enger Substanz ass d'Mass (a Gramm) vun engem Mol vun där Substanz. Fir d'molare Mass vun engem Element ze berechnen, multiplizéiert seng Atommass mam Gramm-pro-Mol Konversiounsfaktor (g / mol).
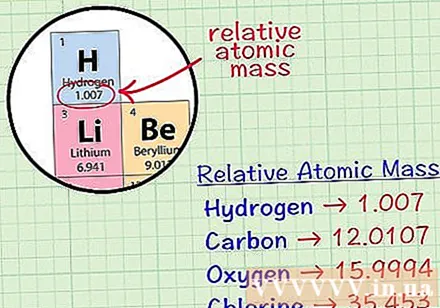
Fannt den duerchschnëttleche kubesche Atom vun engem Element. Den Duerchschnëttsmassatoom vun engem Element ass déi duerchschnëttlech Mass, an atomare Eenheeten, an enger Probe déi all d'Isotopen vun dësem Element enthält. Dës Informatioun gëtt dacks op de periodeschen Dësch vun Elementer uginn. Wann Dir en Element lokaliséiert, kënnt Dir en duerchschnëttlecht kubescht Atom fannen dat just ënner dem chemesche Symbol vum Element geschriwwe gëtt. Dëse Wäert ass net eng ganz Zuel, awer eng Zuel mat Dezimalzuelen.- Zum Beispill mat Waasserstoff ass den Duerchschnëttsmassatoom 1,007; Den duerchschnëttleche kubesche Atom vu Kuelestoff ass 12.0107; Den Duerchschnëttsmassatoom vu Sauerstoff ass 15.9994; Chlor huet eng duerchschnëttlech Atommass vu 35.453.

Multiplizéiert den duerchschnëttleche Massatom mat der Molmassekonstant. D'Eenheet vum molare Glid ass definéiert als 0,001 Kilogramm pro Mol, oder 1 Gramm pro Mol. D'Produkt vum mëttelmassegen Atom an d'molare Massekonstant konvertéiert d'Eenheet vun der Atommass a Gramm pro Mol, sou datt d'Molermass vu Waasserstoff 1,007 Gramm pro Mol ass, Kuelestoff ass 12. , 0107 Gramm pro Mol, Sauerstoff ass 15.9995 Gramm pro Mol, an dee vu Chlor ass 35.453 Gramm pro Mol.- E puer Elementer existéieren an der Natur als Moleküle besteet aus zwee oder méi vun de selwechten Atomer. Dat ass, wann Dir d'molare Mass vu Verbindungen aus méi wéi engem Atom, wéi Waasserstoffgas, Sauerstoffgas oder Chlorgas auszerechnen wëllt, musst Dir déi duerchschnëttlech Atommass vun der Verbindung bestëmmen an dëse Wäert multiplizéieren. mat der Molmassekonstant, '' da '' multiplizéiert Dir dat Produkt dat Dir just mat 2 fonnt hutt.
- Mat H2: 1.007 x 2 = 2.014 Gramm pro Mol; fir O2: 15.9994 x 2 = 31.9988 Gramm pro Mol; a Cl2: 35 453 x 2 = 70 096 Gramm pro Mol.
Method 2 vun 2: Berechent déi molmass vun der Verbindung

Bestëmmt d'Strukturformel vun der Verbindung. D'Strukturformel vun enger Substanz gëtt d'Atomzuel vun all Element, dat dës Verbindung ausmécht. (Dës Informatioun ass an alle Referenzbicher verfügbar). Zum Beispill ass d'chemesch Formel vun Salzsäure HCl; vu Glukos ass C6H12O6. Mat dëser struktureller Formel kënne mir d'Zuel vun all Atomtyp bestëmmen, déi d'Verbindung ënnersicht.- Wou HCl ee Waasserstoffatom an ee Chloratom huet.
- Glukos Zocker Molekül C6H12O6 Et gi 6 Kuelestoffatomer, 12 Waasserstoffatomer a 6 Sauerstoffatomer.
Bestëmmt den Duerchschnëttsmassatoom vun all Bestanddeel. Benotzt de periodeschen Dësch fir den Duerchschnëttsmassatoom vun all Element an der Verbindung ze fannen. Den Duerchschnëttsmassatoom gëtt normalerweis ënner dem chemesche Symbol vum Element op dem periodeschen Dësch geschriwwen. Ähnlech wéi d'Berechnung vun der Molmass vun engem Element multiplizéiert den Duerchschnëttsmassatoom mat 1 Gramm / Mol.
- Den Duerchschnëttsmassatoom vun den Elementer déi Salzsaier bilden ass wéi follegt: Waasserstoff 1,007 g / mol a Chlor 35,453 g / mol.
- Den Duerchschnëttsmassatoom vun den Elementer déi d'Glukosemolekül ausmaachen ass: Kuelestoff, 12.017 g / mol; Waasserstoff, 1.007 g / mol; a Sauerstoff, 15,9995 g / mol.
Berechent d'molare Mass vun all Komponentelement. Multiplikéiere vum Massatom vun engem Element mat der Zuel vun den Atomer, déi et zu enger Verbindung bäidréit, gëtt d'Duerchschnëttsmass vum Element an der Verbindung.
- Am Fall vun Salzsaier, HCl, ass d'Molmass vum Element Waasserstoff 1,007 g / mol, an déi vu Chlor ass 35,453 g / mol.
- Am Fall vu Glukos, C6H12O6, D'molare Mass vun all Element ass wéi follegt: Kuelestoff, 12.0107 x 6 = 72.0642 g / mol; Waasserstoff, 1.007 x 12 = 12.084 g / mol; Sauerstoff, 15.9995 x 6 = 95.9964 g / mol.
Total Molmass vun de Bestanddeeler. Déi gesamt Molmass vun de Kompostéierelementer ass d'molare Mass vun der Verbindung.Am virege Schrëtt hu mir d'molare Mass vun all Element präsent an der Verbindung berechent, an dësem Schrëtt musse mir just all dës Wäerter zesummefügen.
- Molmass vu Salzsaier ass 1,007 + 35,453 = 36,460 g / mol. 36,46 Gramm ass d'Mass vun 1 Mol Salzsaier.
- Molmass vu Glukos ass 72,0642 + 12,084 + 95,9964 = 180,1446 g / mol. Also all Mol Glukos huet eng Mass vun 180,14 Gramm.
Berodung
- Och wann an de meeschte Fäll den Duerchschnëttsmassatoom op deen noosten 1 Deel 1000 (4 Dezimalplazen) opgeholl gëtt, a Laboratoiren gëtt d'Molmass dacks op 2 Dezimalplaze reduzéiert heiansdo souguer manner, fir grouss Molekülen. Dofir, am Labo Fall, kann d'Molermass vu Salzsaier als 36,46 Gramm pro Mol geschriwwe ginn, fir Glukos 180,14 Gramm pro Mol.
Wat Dir braucht
- Chemescht Referenzbuch oder periodesch Tabelle vun Elementer
- Computer