Auteur:
Eric Farmer
Denlaod Vun Der Kreatioun:
10 Mäerz 2021
Update Datum:
1 Juli 2024
Inhalt
- Schrëtt
- Method 1 vun 2: Bestëmmung vun der Unzuel vun Neutronen an Atomer (net Isotopen)
- Method 2 vun 2: Bestëmmung vun der Unzuel vun Neutronen an Isotopen
- Tipps
An Atomer vum selwechte Element ass d'Zuel vu Protonen konstant, wärend d'Zuel vun den Neutronen ka variéieren.Wann Dir wësst wéivill Neutronen e bestëmmten Atom enthält, kënnt Dir bestëmmen ob et e reegelméissegen Atom oder eng Isotop ass déi manner oder méi Neutronen wäert hunn. D'Zuel vun den Neutronen an engem Atom ze bestëmmen ass zimmlech einfach. Alles wat Dir maache musst fir d'Zuel vun den Neutronen an engem Atom oder Isotop ze berechnen ass eis Instruktiounen ze verfollegen an de Periodesystem praktesch ze halen.
Schrëtt
Method 1 vun 2: Bestëmmung vun der Unzuel vun Neutronen an Atomer (net Isotopen)
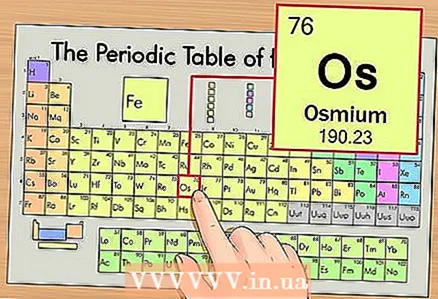 1 Fannt d'Element op der periodescher Tabelle. Als Beispill wäerte mir den Osmium (Os) berücksichtegen, deen an der sechster Period ass (sechster Zeil vun uewen).
1 Fannt d'Element op der periodescher Tabelle. Als Beispill wäerte mir den Osmium (Os) berücksichtegen, deen an der sechster Period ass (sechster Zeil vun uewen).  2 Fannt d'Atomenummer vum Element. Dëst ass, an der Regel, déi bemierkbarst Zuel an der Zell vun engem Element a läit normalerweis iwwer säi Symbol (an der Versioun vum Periodesystem, dat mir an eisem Beispill benotzen, ginn et keng aner Zuelen). D'Atomzuel ass d'Zuel vu Protonen an engem Atom vun deem Element. Fir Osmium ass dës Zuel 76, dat heescht, et gi 76 Protonen an engem Osmiumatom.
2 Fannt d'Atomenummer vum Element. Dëst ass, an der Regel, déi bemierkbarst Zuel an der Zell vun engem Element a läit normalerweis iwwer säi Symbol (an der Versioun vum Periodesystem, dat mir an eisem Beispill benotzen, ginn et keng aner Zuelen). D'Atomzuel ass d'Zuel vu Protonen an engem Atom vun deem Element. Fir Osmium ass dës Zuel 76, dat heescht, et gi 76 Protonen an engem Osmiumatom. - D'Zuel vu Protonen ass onverännert, an dëst ass wat en Element en Element mécht.
 3 Fannt d'Atommass vun engem Element. Dës Nummer gëtt normalerweis ënner dem Element Symbol fonnt. Notéiert w.e.g. datt an der Versioun vum Periodesystem an eisem Beispill d'Atommass net gëtt (dëst ass net ëmmer de Fall; a ville Versioune vum Periodesystem gëtt d'Atommass uginn). D'Atommass vum Osmium ass 190,23.
3 Fannt d'Atommass vun engem Element. Dës Nummer gëtt normalerweis ënner dem Element Symbol fonnt. Notéiert w.e.g. datt an der Versioun vum Periodesystem an eisem Beispill d'Atommass net gëtt (dëst ass net ëmmer de Fall; a ville Versioune vum Periodesystem gëtt d'Atommass uginn). D'Atommass vum Osmium ass 190,23.  4 Ronn d'Atommass op déi nootste ganz Zuel. An eisem Beispill ass 190.23 op 190 ofgerënnt.
4 Ronn d'Atommass op déi nootste ganz Zuel. An eisem Beispill ass 190.23 op 190 ofgerënnt. - Atommass ass déi duerchschnëttlech Unzuel vun Isotopen vun engem bestëmmten Element, normalerweis gëtt se net als Ganzt ausgedréckt.
 5 Zitt d'Atommass vun der Atommass of. Well Protonen an Neutronen den absoluten Deel vun der Atommass ausmellen, gëtt d'Zuel vun de Protonen ofgezunn (dat heescht d'Atommass, déi gläich ass mat der Unzuel vun de Protonen) vun der Atommass d'Zuel vun den Neutronen am Atom ofginn. D'Zuelen nom Dezimalpunkt bezéien sech op déi ganz kleng Mass vun Elektronen an engem Atom. An eisem Beispill: 190 (Atomgewiicht) - 76 (Zuel vu Protonen) = 114 (Zuel vun Neutronen).
5 Zitt d'Atommass vun der Atommass of. Well Protonen an Neutronen den absoluten Deel vun der Atommass ausmellen, gëtt d'Zuel vun de Protonen ofgezunn (dat heescht d'Atommass, déi gläich ass mat der Unzuel vun de Protonen) vun der Atommass d'Zuel vun den Neutronen am Atom ofginn. D'Zuelen nom Dezimalpunkt bezéien sech op déi ganz kleng Mass vun Elektronen an engem Atom. An eisem Beispill: 190 (Atomgewiicht) - 76 (Zuel vu Protonen) = 114 (Zuel vun Neutronen). 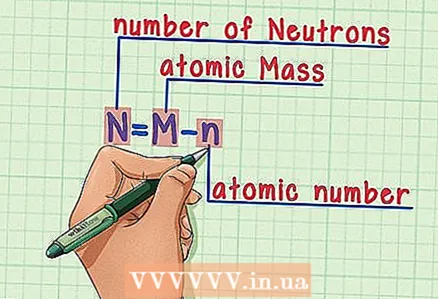 6 Denkt un d'Formel. Fir d'Zuel vun den Neutronen an der Zukunft ze fannen, benotzt einfach dës Formel:
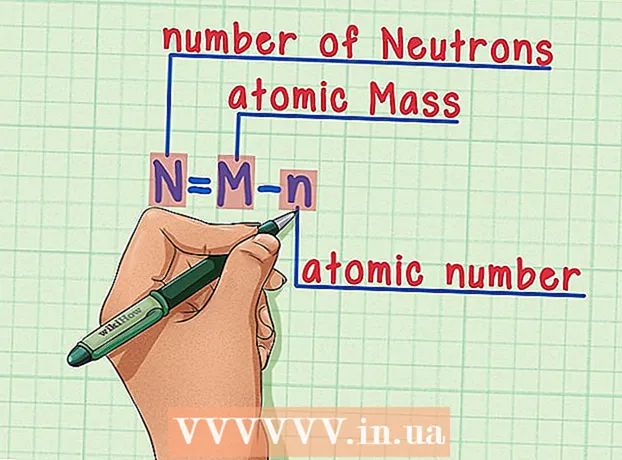
6 Denkt un d'Formel. Fir d'Zuel vun den Neutronen an der Zukunft ze fannen, benotzt einfach dës Formel: - N = M - n
- N = Zuel vun Neutronen
- M = Atommass
- n = atomarer Zuel
- N = M - n
Method 2 vun 2: Bestëmmung vun der Unzuel vun Neutronen an Isotopen
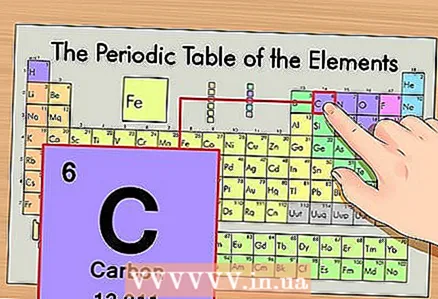 1 Fannt d'Element op der periodescher Tabelle. Als Beispill wäerte mir d'Isotop vu Kuelestoff 14C berücksichtegen. Well den net-isotopesche Kuelestoff 14C just Kuelestoff C ass, fënnt Kuelestoff op der periodescher Tabell (zweeter Period oder zweeter Zeil vun uewen).
1 Fannt d'Element op der periodescher Tabelle. Als Beispill wäerte mir d'Isotop vu Kuelestoff 14C berücksichtegen. Well den net-isotopesche Kuelestoff 14C just Kuelestoff C ass, fënnt Kuelestoff op der periodescher Tabell (zweeter Period oder zweeter Zeil vun uewen). 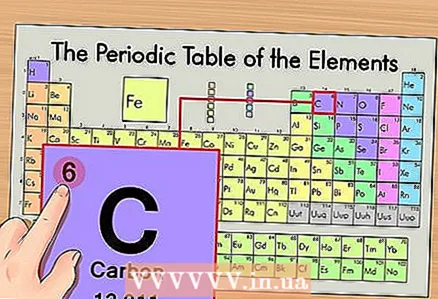 2 Fannt d'Atomenummer vum Element. Dëst ass, an der Regel, déi bemierkbarst Zuel an der Zell vun engem Element a läit normalerweis iwwer säi Symbol (an der Versioun vum Periodesystem, dat mir an eisem Beispill benotzen, ginn et keng aner Zuelen). D'Atomenummer ass d'Zuel vu Protonen an engem Atom vun deem Element. Kuelestoff ass Nummer 6, dat heescht datt ee Kuelestoff sechs Protone huet.
2 Fannt d'Atomenummer vum Element. Dëst ass, an der Regel, déi bemierkbarst Zuel an der Zell vun engem Element a läit normalerweis iwwer säi Symbol (an der Versioun vum Periodesystem, dat mir an eisem Beispill benotzen, ginn et keng aner Zuelen). D'Atomenummer ass d'Zuel vu Protonen an engem Atom vun deem Element. Kuelestoff ass Nummer 6, dat heescht datt ee Kuelestoff sechs Protone huet.  3 Fannt d'Atommass. Am Fall vun Isotopen ass dëst ganz einfach ze maachen, well se no hirer Atommass benannt ginn. An eisem Fall huet Kuelestoff 14C eng Atommass vun 14. Elo kenne mir d'Atommass vum Isotop; de spéideren Berechnungsprozess ass d'selwecht wéi fir d'Zuel vun den Neutronen an Atomer ze bestëmmen (net Isotopen).
3 Fannt d'Atommass. Am Fall vun Isotopen ass dëst ganz einfach ze maachen, well se no hirer Atommass benannt ginn. An eisem Fall huet Kuelestoff 14C eng Atommass vun 14. Elo kenne mir d'Atommass vum Isotop; de spéideren Berechnungsprozess ass d'selwecht wéi fir d'Zuel vun den Neutronen an Atomer ze bestëmmen (net Isotopen).  4 Zitt d'Atommennummer vun der Atommass of. Well Protonen an Neutronen den absoluten Deel vun der Atommass ausmellen, gëtt d'Zuel vun de Protonen ofgezunn (dat heescht d'Atommass, déi gläich ass mat der Unzuel vun de Protonen) vun der Atommass d'Zuel vun den Neutronen am Atom ofginn. An eisem Beispill: 14 (Atommass) - 6 (Zuel vu Protonen) = 8 (Zuel vun Neutronen).
4 Zitt d'Atommennummer vun der Atommass of. Well Protonen an Neutronen den absoluten Deel vun der Atommass ausmellen, gëtt d'Zuel vun de Protonen ofgezunn (dat heescht d'Atommass, déi gläich ass mat der Unzuel vun de Protonen) vun der Atommass d'Zuel vun den Neutronen am Atom ofginn. An eisem Beispill: 14 (Atommass) - 6 (Zuel vu Protonen) = 8 (Zuel vun Neutronen). 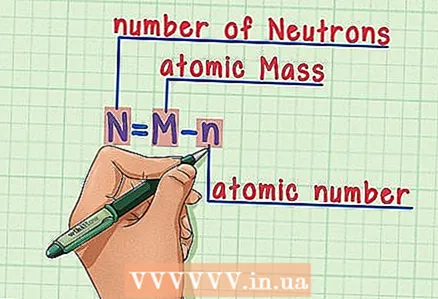 5 Denkt un d'Formel. Fir d'Zuel vun den Neutronen an der Zukunft ze fannen, benotzt einfach dës Formel:
5 Denkt un d'Formel. Fir d'Zuel vun den Neutronen an der Zukunft ze fannen, benotzt einfach dës Formel: - N = M - n
- N = Zuel vun Neutronen
- M = Atommass
- n = atomarer Zuel
- N = M - n
Tipps
- Protonen an Neutronen bilden bal déi absolut Mass vun Elementer aus, während Elektronen an aner Partikelen eng extrem onbedeitend Mass ausmaachen (dës Mass tendéiert op Null).Well ee Proton ongeféier déiselwecht Mass huet wéi een Neutron, an d'Atomzuel d'Zuel vu Protonen ass, kënnt Dir d'Zuel vun de Protone vun der Gesamtmass einfach ofsetzen.
- Osmium - e Metal an engem festen Zoustand bei Raumtemperatur, krut säin Numm vum griichesche Wuert "osme" - Geroch.
- Wann Dir net sécher sidd wat eng Zuel am Periodesystem heescht, erënners du: den Dësch ass normalerweis ronderëm eng Atomzuel gebaut (dat heescht d'Zuel vu Protonen), déi bei 1 (Waasserstoff) ufänkt an eng Eenheet vu lénks no riets wiisst , Enn mat 118 (Oganesson). Dëst ass well d'Zuel vu Protonen an engem Atom d'Element selwer bestëmmt, an esou eng Nummer ass den einfachsten Wee fir d'Elementer ze organiséieren (zum Beispill, en Atom mat 2 Protonen ass ëmmer Helium, sou wéi en Atom mat 79 Protonen ëmmer Gold ass ).